安徽中医药大学王琪/程志非/桂双英开发了一种工程化细胞外囊泡纳米制剂用于重塑帕金森病脑免疫微环境!
虽然对小胶质细胞的常规干预可以在短期内减轻神经炎症,但外周炎症细胞引起的免疫反应可以持续发生,过度激活帕金森病(PD)的免疫微环境。
2024年8月15日,安徽中医药大学王琪、程志非、桂双英共同通讯在ACS Nano(IF=15.8)在线发表题为“Engineered Extracellular Vesicle-Based Nanoformulations That Coordinate Neuroinflammation and Immune Homeostasis, Enhancing Parkinson’s Disease Therapy”的研究论文,该研究设计了工程化细胞外囊泡制剂(EVN)来解决帕金森病治疗的多个障碍。
具体来说,通过将富含CCR2的间充质干细胞衍生的细胞外囊泡(MSCCCR2 EVs)包覆在负载二氢丹参酮I的纳米载体(MSeN-DT)外,制备得到EVN。MSCCCR2 EVs(EVN的外壳显示出对黑质中特定趋化因子CCL2的特异性靶向,使其能够阻断外周炎症细胞的浸润。有趣的是,MSeN-DT(EVN的核心)可以通过抑制小胶质细胞中的铁死亡来增强Nrf2-GPX4通路,从而抑制炎症发生源头。帕金森病小鼠模型中,EVN治疗效果显著,抑制了外周炎症细胞浸润,精确调节了黑质中的炎症小胶质细胞,并促进行为改善、修复受损神经元。通过缓解炎症和调节免疫稳态,该方法可以重塑帕金森病的免疫微环境,从而连接内部抗炎和外部免疫,打破免疫过度激活的恶性循环,是一种全面治疗帕金森病的参考范例。

帕金森病(PD)是最常见的神经退行性疾病之一,其特征是多巴胺能神经元进行性损伤和黑质(SN)中α-突触核蛋白(α-syn)的异常积累。脑免疫微环境过度激活是帕金森病快速发作的关键因素,驻留小胶质细胞的神经炎症和外周炎症细胞持续浸润则加速该病进展。激活下游抗炎信号通路(如NF-κB)或利用纳米酶的生物催化等策略已经用来解决小胶质细胞中过度活性氧(ROS)的问题,但如果不及时预防外周炎细胞浸润导致ROS产生的源头或免疫下降,就难以达到帕金森病治疗的目的。因此,需要一种“内部”抑制小胶质细胞产生炎症的源头、“外部”阻断炎症细胞浸润的综合性疗法,恢复异常的免疫紊乱。
核因子红系2相关因子2(Nrf2)作为调节蛋白在细胞氧化还原过程中起着关键作用,通过Keap1-Nrf2系统参与调节各种下游抗炎蛋白,从而抑制α-syn的异常聚集。越来越多的证据表明,Nrf2可以激活帕金森病中的一种铁死亡相关蛋白(谷胱甘肽过氧化物酶4,GPX4),该蛋白可抑制由铁依赖性脂质过氧化引起的程序性细胞死亡。然而,帕金森病中Nrf2的细胞质水平显著降低,限制了其介导抗炎信号通路的能力。理想情况下,Nrf2激活剂不仅可以确保其从细胞质中的Keap1中释放出来,还可以调节细胞核中的输入和输出信号通路,促进Nrf2核积累。天然化合物,特别是具有多靶点和多通路药理学的植物源性Nrf2激活剂,具有完全激活Nrf2的潜力。虽然其他植物来源的Nrf2激活剂通常调节单一因子,但从丹参中提取的活性成分二氢丹参酮I(DT)可以上调核输入信号并阻断核输出信号,协同解决Nrf2激活过程中的多个因素。然而,DT是一种疏水性小分子,在全身给药时药代动力学和生物利用度较差。因此,开发基于DT的靶向纳米递送系统对于有效激活Nrf2和阻止帕金森病中ROS的产生至关重要。
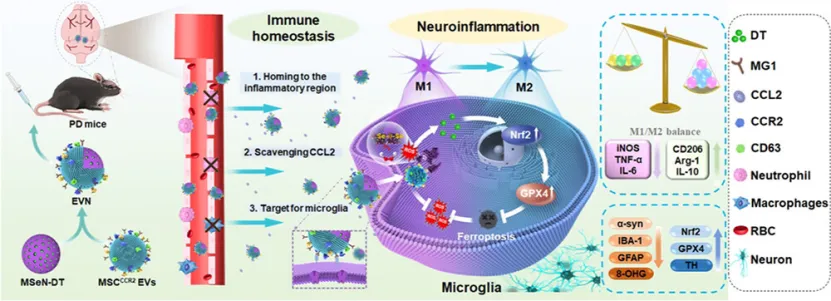 过表达CCR2的工程化细胞外囊泡纳米制剂的制备及其治疗帕金森病示意图(图源自ACS Nano)
过表达CCR2的工程化细胞外囊泡纳米制剂的制备及其治疗帕金森病示意图(图源自ACS Nano)
此外,脑免疫功能障碍也会加速帕金森病的恶化。其中,C-C基序趋化因子配体2(CCL2)是活化的小胶质细胞或星形胶质细胞分泌的重要趋化因子,与C-C趋化因子受体2型(CCR2)特异性结合。过表达CCR2的外周中性粒细胞或巨噬细胞持续募集到帕金森病的损伤中心,促进小胶质细胞释放更多的炎症因子,诱导更多的免疫细胞活化,导致帕金森病脑免疫失衡加剧。因此,阻断CCR2-CCL2轴是预防外周炎症细胞浸润并维持脑免疫稳态的有效方法。
该研究设计了一种工程化EV纳米制剂(EVN),通过调节炎症和免疫稳态实现帕金森病协同治疗。富含CCR2的间充质干细胞衍生的细胞外囊泡(MSCCCR2 EVs)为壳,二硒化物桥联介孔二氧化硅纳米颗粒负载DT(MSeN-DT)为核,得到EVN。通过基因转染上调MSCCCR2 EVs上CCR2的表达,不仅可以作为“纳米导航者”归巢到脑内的炎症部位,还可以作为“纳米诱饵”中和大量的CCL2,从而阻断外周炎症细胞的浸润。然后在MSCCCR2 EVs表面修饰MG1肽,以准确识别复杂神经系统中的M1小胶质细胞。炎性小胶质细胞摄取EVN后,MSeN-DT在高ROS环境下释放DT,通过增强Nrf2的表达有效抑制ROS的产生,还能够激活Nrf2-GPX4通路来抑制铁死亡,这两种途径共同促进了小胶质细胞中抗炎表型的转换。总得来说,该研究证明EVNs提供了一种帕金森病的综合性疗法,整合了趋化性和靶向性,减轻炎症并调节免疫稳态。该研究报道了一种连接内部和外部免疫的协同治疗策略,以重塑帕金森病中过度激活的大脑微环境。
【本文来源】iNature 作者:椰子
【原文链接】
https://mp.weixin.qq.com/s/SEyyJxhI0qZ4AXhtdUt8NQ
【特别声明】本文转载仅仅是出于传播信息的需要,并不意味着代表本网站观点或证实其内容的真实性;如其他媒体、网站或个人从本网站转载使用,须保留本网站注明的“来源”,并自负版权等法律责任;作者如果不希望被转载等事宜,请与我们接洽。